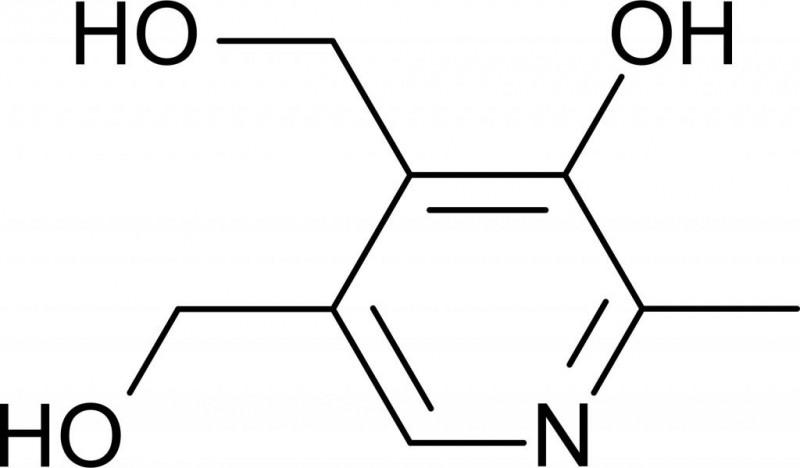
Аденозинмонофосфат
Содержание:
функции
АТФ играет незаменимую роль в энергетическом обмене практически всех живых организмов. По этой причине его часто называют энергетической валютой, поскольку его можно постоянно тратить и пополнять всего за несколько минут..
Прямой или косвенный, АТФ обеспечивает энергию для сотен процессов, в дополнение к действию в качестве донора фосфата.
В общем, АТФ действует как сигнальная молекула в процессах, происходящих внутри клетки, необходимо синтезировать компоненты ДНК и РНК и для синтеза других биомолекул участвует в трафике через мембраны, среди других.
Использование АТФ можно разделить на основные категории: транспорт молекул через биологические мембраны, синтез различных соединений и, наконец, механическая работа..
Функции СПС очень широки. Кроме того, он вовлечен в так много реакций, что было бы невозможно назвать их всех. Поэтому мы обсудим три конкретных примера, иллюстрирующих каждое из трех упомянутых применений..
Энергоснабжение для транспорта натрия и калия через мембрану
Ячейка является чрезвычайно динамичной средой, которая требует поддержания определенных концентраций. Большинство молекул не попадают в клетку случайно или случайно. Для того чтобы молекула или вещество могли проникнуть внутрь, оно должно делать это посредством своего конкретного переносчика..
Транспортеры — это белки, которые пересекают мембрану и функционируют как клеточные «привратники», контролирующие поток материалов. Следовательно, мембрана является полупроницаемой: она позволяет некоторым соединениям проникать, а другим — нет..
Одним из самых известных видов транспорта является натриево-калиевый насос. Этот механизм классифицируется как активный транспорт, так как движение ионов происходит против их концентрации, и единственный способ выполнить это движение — ввести энергию в систему в форме АТФ..
Подсчитано, что одна треть АТФ, образующегося в клетке, используется для поддержания работы насоса. Ионы натрия постоянно перекачиваются на поверхность клетки, а ионы калия — наоборот.
Логично, что использование АТФ не ограничивается транспортировкой натрия и калия. Есть другие ионы, такие как кальций, магний и другие, которые нуждаются в этой энергетической валюте, чтобы войти.
Участие в синтезе белка
Молекулы белка образованы аминокислотами, связанными между собой пептидными связями. Для их формирования требуется разрыв четырех высокоэнергетических связей. Другими словами, для образования белка средней длины необходимо гидролизовать значительное количество молекул АТФ..
Синтез белков происходит в структурах, называемых рибосомами. Они способны интерпретировать код, которым обладает РНК-мессенджер, и транслировать его в аминокислотную последовательность, АТФ-зависимый процесс.
В наиболее активных клетках синтез белка может направлять до 75% АТФ, синтезированного в этой важной работе. С другой стороны, клетка не только синтезирует белки, она также нуждается в липидах, холестерине и других необходимых веществах, и для этого требуется энергия, содержащаяся в связях АТФ.
С другой стороны, клетка не только синтезирует белки, она также нуждается в липидах, холестерине и других необходимых веществах, и для этого требуется энергия, содержащаяся в связях АТФ..
Обеспечить энергию для передвижения
Механическая работа является одной из важнейших функций СПС. Например, чтобы наше тело могло выполнять сокращение мышечных волокон, необходимо наличие большого количества энергии..
В мышцах химическая энергия может быть преобразована в механическую энергию благодаря реорганизации протеинов с сокращающей способностью, которые ее формируют. Длина этих структур изменена, укорочена, что создает напряжение, которое приводит к генерации движения.
У других организмов движение клеток также происходит благодаря наличию АТФ. Например, движение ресничек и жгутиков, которое позволяет перемещать определенные одноклеточные организмы, происходит посредством использования АТФ.
Другое конкретное движение — амебное, которое включает в себя выпячивание псевдоподы на концах клетки. Несколько типов клеток используют этот механизм локомоции, включая лейкоциты и фибробласты.
В случае половых клеток локомоция необходима для эффективного развития эмбриона. Эмбриональные клетки перемещаются на значительные расстояния от места их происхождения до региона, в котором они должны создавать специфические структуры..
Синтез АТФ и ГТФ
Синтез ГТФ осуществляется в 2 стадии посредством переноса макроэргических фосфатных групп от АТФ (рис.6).
|
Нуклеозидмоно- |
Нуклеозидди- |
|||||||
|
ГМФ |
фосфат-киназа |
ГДФ |
фосфат-киназа |
ГТФ |
||||
|
АТФ |
АДФ |
АТФ |
АДФ |
|||||
|
АМФ |
АДФ |
АТФ |
||||||
|
Нуклеозидмоно- |
Окислительное |
|||||||
|
фосфат-киназа |
фосфорилирование |
Рис.6. Образование пуриновых нуклеотидтрифосфатов
Синтез АТФ происходит несколько иначе. АДФ из АМФ образуется также за счет макроэргических связей АТФ. Для синтеза же АТФ из АДФ в клетке есть специальный фермент – АТФ-синтетаза, находящаяся в мембране митохондрий и образованиt АТФ происходит в процессе окислительного фосфорилирования.
УГЛЕВОДЫ
З.6.4.2. Гексозомонофосфатный путь распада углеводов
Незначительная часть глюкозы (5 — 10 %) в организме подвергается распаду по ГМФ-пути (в основном в печени, надпочечниках, эритроцитах, жировой ткани).
ГМФ — путь можно разделить на два этапа, причем первый этап протекает обязательно, а второй — не всегда.
Первый этап начинается с перехода глюкозы в активную форму — глюкозо-6-фосфат, от которого затем отщепляются молекула углекислого газа и две пары атомов водорода, присоединяющиеся к коферменту НАДФ (никотинамидадениндинук-леотидфосфату). Конечным продуктом первого этапа является рибозо-5 — фосфат (моносахарид, содержащий пять атомов углерода и связанный с остатком фосфорной кислоты, т. е. пентозофосфат).
1. Глюкоза + АТФ —> Глюкозо-6-фосфат + АДФ.
2. Глюкозо-6 — фосфат + 2НАДФ —> Рибозо-5 — фосфат + 2НАДФ • Н2 + СO2.
Образовавшийся рибозо-5 — фосфат используется для синтеза нуклеотидов, из которых далее образуются нуклеиновые кислоты и коферменты (например, коферменты А, НАД, НАДФ, ФМН, ФАД). Кофермент НАДФ • Н2 поставляет атомы водорода для различных синтетических процессов, в том числе для синтеза жирных кислот и холестерина.
Второй этап ГМФ — пути реализуется тогда, когда рибозо-5 — фосфат полностью не расходуется. Неиспользованные молекулы реагируют друг с другом, в качестве промежуточных продуктов появляются моносахариды с различным числом атомов углерода (триозы, тетрозы, пентозы, те птозы).
В результате образуются 5 молекул глюкозо-6 — фосфата:
6 рибозо-5 — фосфат —> 5 глюкозо-6 — фосфат.
Второй этап данного распада глюкозы имеет циклический характер, поэтому его часто называют пентозным циклом.
Объединив оба этапа, можно получить общую схему пентозного цикла (рис. 16).
Рис. 16. Общая схема пентозного цикла
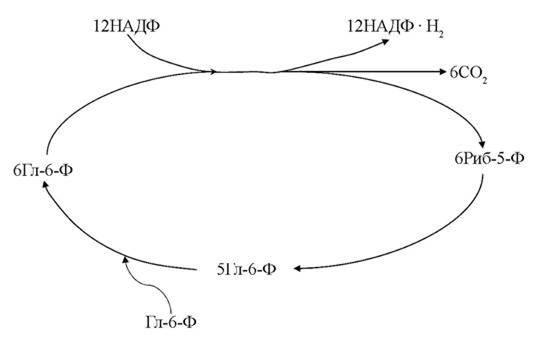
ГМФ — путь распада глюкозы наблюдается в цитоплазме клеток, имеет анаболическое назначение и обеспечивает различные синтезы рибозой и водородом в форме НАДФ • Н2.
Применение
В отличие от глутаматов, влияющих на мясной вкус, добавка E 626 модифицирует сладкий и соленый вкус и усиливает различные ароматы.
Продукт входит в список разрешенных, но пищевая промышленность его практически не применяет. Причина в слабой растворимости вещества в воде.
Спросом пользуются соли гуаниловой кислоты — гуанилаты.
В Кодексе Алиментариус добавка Е 626 разрешена в супах и бульонах, произведенных по стандарту GMP (Good Manufacturing Practice, международный стандарт, определяющий требования безопасности в производстве лекарств и продуктов питания).
В России усилитель вкуса и аромата (не более 500 мг/кг) разрешено добавлять в следующие продукты:

- приправы и пряности;
- готовые закуски;
- соусы;
- вермишель быстрого приготовления;
- суповые концентраты.
Гуаниловая кислота — обязательный ингредиент большинства блюд японской кухни. Она входит в состав знаменитого бульона даси, призванного подчеркивать естественный вкус входящих в него продуктов.
Добавка E 626 разрешена в России, странах ЕАЭС и Евросоюза, США, Китае. Запрещена к использованию в Новой Зеландии и Австралии. Допустимая доза неограничена.
В медицине препараты на основе нуклеиновых кислот животного и микробного происхождения применяют для лечения аутоиммунных и онкологических заболеваний, бактериальных и вирусных инфекций.
ГБФ-путь (гексозобифосфатный путь распада углеводов)
Три этапа ГБФ-пути. 1-й этап протекает в цитоплазме, дает 8 молекул АТФ при распаде 1 молекулы глюкозы или 9 АТФ при распаде одного глюкозного фрагмента гликогена. Заканчивается образованием 2 молекул пирувата (ПВК), 2-й и 3-й этапы (исключительно аэробные) — в митохондриях с обязательным участием кислорода, дают 30 АТФ на одну молекулу глюкозы. 2-й этап — окислительное декарбоксилирование пирувата, катализируется пируватдегидрогеназным комплексом. От молекулы пирувата отнимаются 2 атома водорода, и пируват превращается в ацетил-кофермент А (АцКоА), одновременно происходит отщепление СО2. 2 атома водорода идут на НАД, а затем по цепи митохондриального окисления передаются на О2 с образованием Н2О и 3 молекул АТФ. В расчете на 1 молекулу исходной глюкозы 2-й этап дает 6 АТФ. 3-й этап — цикл трикарбоновых кислот (ЦТК) — вступает молекула АцетилКоА, образовавшегося в результате 2-го этапа. АцКоА полностью расщепляется до СО2 и Н2О. При этом образуется 12 АТФ в расчете на 1 молекулу АцКоА, вступившую в цикл. Если рассчитать на 1 молекулу глюкозы, то на 3-м этапе образуется 24 АТФ.
Последовательность реакций 1-го этапа ГБФ-пути. 1-я реакция — гексокиназа (ГК) работает, чтобы ослабить прочную молекулу глюкозы. 2-я реакция —изомеризации. 3-я реакция — фруктозо-6-фосфат еще более ослабляется фосфофруктокиназой (ФФК) и образуется фруктозо-1,6-бисфосфат. Фосфофрук-токиназа — ключевой фермент ГБФ-пути. Избыток АТФ и избыток цитрата сильно ингибируют ФФК. В этих условиях лимитирующим ферментом ГБФ-пути вместо гексокиназы становится ФФК. Если нет избытка АТФ и цитрата, а есть избыток АДФ (аденозиндифосфата), то АДФ активирует ФФК (фосфофруктокиназой), и тогда скорость всего ГДФ-пути лимитируется гексокиназой. В результате фосфофруктокиназной реакции молекула фруктозо-1,6-бифосфата ослабляется настолько, что сразу распадается на 2 триозы при участии альдолазы (4-я реакция). 5-я реакция: переход ФДА в ФГА (фосфоглицериновый альдегид) с помощью триозофосфатизомеразы. В 6-ю реакцию ГБФ-пути вступает только ФГА. В результате уменьшается его концентрация и равновесие 5-й реакции сдвигается в сторону образования ФГА. Постепенно весь ФДА переходит в ФГА, и поэтому количество АТФ, синтезировавшееся в последующих реакциях ГБФ-пути, мыучитываем в расчете на 2 молекулы ФГА и других промежуточных метаболитов, которые из него образуются. 7-я реакция: субстратное фосфорилирование. Фосфат с макроэргической связью передается на АДФ с образованием АТФ. В результате в молекуле фосфоглицериновой кислоты остается один остаток фосфорной кислоты. 8-я реакция: фосфат переносится из 3-го во 2-е положение, и образуется 2-фосфоглицериновая кислота. 9-я реакция: от 2-фосфоглицериновой кислоты отнимается Н2О. Получается фосфоенолпируват (ФЕП). 10-я реакция: субстратное фосфорилирование. Фосфат переносится на АДФ с образованием АТФ. Фосфоенолпируват переходит в пировиноградную кислоту.
ГМФ-путь (гексозомонофосфатный путь распада углеводов)
ГБФ-путь протекает в цитоплазме в два этапа: 1) окислительный; 2) неокислительный.
Окислительный этап: 2 реакции окисления гексозофосфата без участия кислорода. Н2 переносится на НАДФ. Затем отщепляется СО2. Образуется молекула пентозо-фосфата, НАДФН2 и молекула СО2. Биологическое значение 1-го этапа ГМФ-пути: 1) происходит прямое окисление глюкозофосфата без участия кислорода; 2) один из главных источников НАДФН2 для клетки.
НАДФН2 образуется в цитоплазме, поэтому не передает свой водород по системе митохондриального окисления на кислород и АТФ не образуется. Водород идет на синтез жирных кислот, холестерина и других стероидов, на монооксигеназные реакции. Образуется СО2 — один из конечных продуктов метаболизма без участия кислорода. Образуются пентозы — строительный материал для синтеза нуклеотидов, коферментов.
Неокислительный этап: совокупность большого количества обратимых реакций. Каждая из них — перенос 2- или 3-углеродного фрагмента с одного моносахарида на другой. Между моносахаридами происходит взаимный обмен частями своих молекул. При этом из пентозофосфатов, вступающих в реакцию, образуются моносахариды с разным числом углеродных атомов — триозы (фосфоглицериновый альдегид), тетрозы, гексозы, гептозы. Реакции катализируются трансальдолазами и транскетолазами. В состав кофермента транскетолаз входит витамин В1 (тиамин). В результате 6 молекул рибозо-5-фосфата превращаются в 5 молекул глюкозо-6-фосфата. Биологическое значение 2-го этапа ГМФ-пути: 1) обеспечивает завершение 1-го этапа (утилизирует продукты 1-го этапа); 2) является источником моносахаридов с разным числом углеродных атомов — строительного материала для разных синтезов, в том числе для синтезов олигосахаридов клеточных рецепторов. Образующийся ФГА — точка сопряжения между ГМФ-путем и некоторыми другими путями метаболизма. Например, ФГА может восстанавливаться до фосфоглицерина, необходимого для синтеза жиров. Фосфоглицерин может окисляться до ФГА. Таким образом, в ходе ГМФ-пути молекулы глюкозы превращаются в молекулы глюкозо-6-фосфата, каждая из которых 2 раза окисляется и дает молекулу рибозо-5-фосфата, 2 молекулы НАДФН2 и 1 молекулу СО2. Затем из каждых 6 молекул рибозо-5-фосфата получается 5 молекул глюкозо-6-фосфата. Эти 5 молекул глюкозо-6-фосфата вместе с еще 1, поступающей дополнительно, опять вступают в ГМФ-путь. Получается цикл. На каждом его «обороте» происходит частичное окисление 6 молекул глюкозо-6-фосфата, т.е. 5 молекул глюкозо-6-фосфата остаются нетронутыми, а 1 молекула полностью расщепляется до СО2 и Н2О.
Итоговое уравнение ГМФ-пути:
С6Н12О6 + 6 Н2О + 12 НАДФ ——> 6 CO2 + 12 НАДФН2.
ГМФ-путь протекает без участия кислорода, при этом половина молекулы кислорода в составе СО2 получается из Н2О. Половина молекулы водорода, попадающей в состав НАДФН2, получается не из глюкозы, а из Н2О, которая вступает в ГМФ-путь на 1-м этапе.
АТФ мышц
Что такое АТФ?
АТФ (аденозинтрифосфат, аденозинтрифосфорная кислота) – основное макроэргическое соединение организма. Состоит из аденина (азотистого основания), рибозы (углевод) и трех последовательно расположенных фосфатных остатков, причем второй и третий фосфатные остатки присоединяются макроэргической связью. Структура АТФ выглядит следующим образом (рис.1).
Рис. 1. Структура АТФ
История открытия АТФ
АТФ был открыт(а) в 1929 году немецким биохимиком Карлом Ломаном (Karl Lohmann) и, независимо Сайрусом Фиске (Cyrus Fiske) и Йеллапрагада Субба Рао (Yellapragada Subba Rao) из Гарвардской медицинской школы. Однако структура АТФ была установлена только спустя несколько лет. Владимир Александрович Энгельгардт в 1935 году показал, что для сокращения мышц необходимо присутствие АТФ. В 1939 году В. А. Энгельгардт совместно со своей женой М. Н. Любимовой предъявили доказательства, что миозин проявляет ферментную активность при этом расщепляется АТФ и высвобождается энергия. Фриц Альберт Липманн (Fritz Albert Lipmann) в 1941 году показал, что АТФ является основным переносчиком энергии в клетке. Ему принадлежит фраза «богатые энергией фосфатные связи». В 1948 году Александр Тодд (Alexander Todd) (Великобритания) синтезировал АТФ. В 1997 году Пол Д. Бойер (Paul D. Boyer) и Джон Э. Уокер (John E. Walker) получили Нобелевскую премию по химии за разъяснение ферментативного механизма, лежащего в основе синтеза АТФ.
Содержание АТФ в мышечных волокнах
Количество АТФ в тканях организма человека относительно невелико, поскольку он (она) в тканях не запасается. В мышечных волокнах содержится 5 ммоль на кг сырой ткани или 25 ммоль на кг сухой мышечной ткани.
Реакция гидролиза
Непосредственным источником энергии при мышечной деятельности является АТФ, который (ая) находится в саркоплазме мышечных волокон. Освобождение энергии происходит в результате реакции гидролиза АТФ.
Гидролиз АТФ – реакция, протекающая в мышечных волокнах, при которой АТФ, взаимодействуя с водой распадается на АДФ и фосфорную кислоту. При этом выделяется энергия. Гидролиз АТФ ускоряется ферментом АТФ-азой. Этот фермент находится на каждой миозиновой головке толстого филамента.
Реакция гидролиза АТФ имеет следующий вид:
АТФ+Н2О→АДФ+Н3РО4 + энергия
В результате гидролиза 1 моль АТФ выделяется энергия, равная 42-50 кДж (10-12 ккал). Скорость протекания реакции гидролиза повышают ионы кальция. Следует отметить, что АДФ (аденозиндифосфат) в мышечных волокнах выполняет роль универсального акцептора (приёмника) высокоэнергетического фосфата и используется для образования АТФ.
Фермент АТФ-аза
Фермент АТФ-аза расположен на миозиновых головках, что играет существенную роль в сокращении мышечных волокон. Активность фермента АТФ-азы лежит в основе классификации мышечных волокон на медленные (I тип), промежуточные (IIA тип) и быстрые (IIB тип).
Химическая энергия, выделяемая в результате гидролиза в мышечных волокнах, расходуется на: сокращение мышечных волокон (взаимодействие белков актина и миозина) и на их расслабление (работу кальциевого и натрий-калиевого насосов). При взаимодействии с актином одна молекула миозина за одну секунду гидролизует 10 молекул АТФ.
Запасы АТФ в мышечных волокнах невелики и могут обеспечить выполнение интенсивной работы в течение 1-2 с. Дальнейшая мышечная деятельность осуществляется благодаря быстрому восстановлению (ресинтезу) АТФ, поэтому при сокращении мышечных волокон в них одновременно протекают два процесса: гидролиз АТФ, дающий необходимую энергию и ресинтез АТФ, восполняющий запасы АТФ в мышечных волокнах.
Ресинтез АТФ
Ресинтез АТФ – синтез АТФ в мышечных волокнах из различных энергетических субстратов во время физической работы. Его формула выглядит следующим образом:
АДФ+фосфат+энергия → АТФ
Ресинтез АТФ может осуществляться двумя путями:
- без участия кислорода (анаэробный путь);
- с участием кислорода (аэробный путь).
Если в саркоплазме мышечных волокон недостаточно АТФ, то затрудняется процесс их расслабления. Возникают судороги.
Более подробно строение и функции мышц описаны в моих книгах «Гипертрофия скелетных мышц человека» и «Биомеханика мышц»
Литература
- Михайлов С.С. Спортивная биохимия. – М.: Советский спорт, 2009.– 348 с.
- Волков Н.И., Несен Э.Н., Осипенко А.А., Корсун С.Н. Биохимия мышечной деятельности.- Киев: Олимпийская литература, 2000.- 504 с.
Макроэргические соединения – химические соединения, содержащие связи, при гидролизе которых происходит освобождение значительного количества энергии.
Регуляция синтеза пуринов
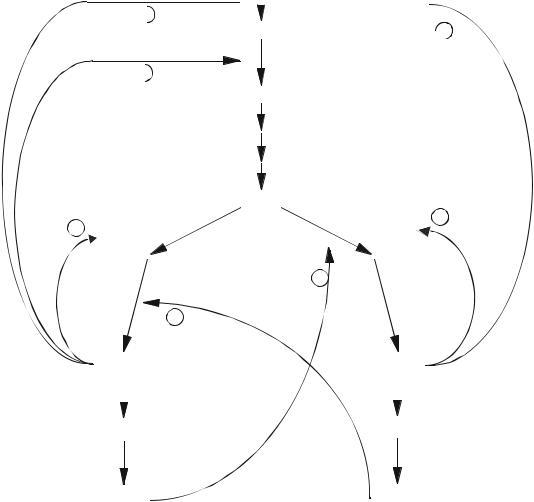
Регуляция синтеза пуринов происходит по механизму обратной отрицательной связи, т.е. продукт реакции (совокупности реакций) ингибирует начальные этапы процесса. Для синтеза пуринов такими ингибиторами являются АМФ и ГМФ. ГМФ блокирует первые две реакции синтеза ИМФ, а также ИМФ-дегидрогеназную реакцию. АМФ блокирует первую реакцию синтеза ИМФ и аденилосукцинатсинтетазную реакцию (рис.7).
Кроме этого, имеется положительная перекрестная регуляция со стороны АТФ и ГТФ, а именно – как участник реакций каждый из них оказывают стимулирующее влияние на синтез другого нуклеотида. Это заключается в том, что АТФ, принимая участие в ГМФ-синтетазной реакции, облегчает синтез ГМФ; в свою очередь, ГТФ является донором энергии для синтеза АМФ, участвуя в аденилосукцинатсинтетазной реакции.
Естественно, что ключевые реакции синтеза пуринов не могли остаться без внимания исследователей и разработчиков новых противоопухолевых средств. Были предложены ингибиторы таких ферментов как ФРПФ-амид-трансфераза (азосерин, диазонорлейцин), ИМФ-дегидрогеназа (микофеноловая кислота, 6-меркаптопурин), аденилосукцинат-лиаза (6-меркаптопурин)
5
Рибозо-5-фосфат
—
—
ФРПФ-синтетаза
ФРПФ —
ФРПФ-амид-ТФ
5-фосфорибозил- амин
|
ИМФ |
— |
|||
|
— ИМФ-дегидрогеназа |
Аденилосукцинат- |
|||
|
синтетаза |
||||
|
ГМФ-синтетаза |
+ |
|||
|
Аденилосукцинат- |
||||
|
+ |
лиаза |
|||
|
ГМФ |
АМФ |
|||
|
ГДФ |
АДФ |
Рис.7. Регуляция синтеза пуриновых оснований