Где используется метиловый или древесный спирт?
Содержание:
- Тяжесть отравления
- Как проверить питьевой или нет в домашних условиях?
- ОПИСАНИЕ
- Виды спирта и характеристики
- Как отличить этиловый спирт от метилового в домашних условиях?
- Что такое летальный синтез?
- Можно ли отравиться этанолом?
- Головы, хвосты и промежуточные примеси
- Отравление этиленгликолем
- Свойства метилового спирта
- Заключение
Тяжесть отравления
Зависит от дозы, индивидуальных биологических особенностей (содержание фермента АДГ генетически ниже в организме северных народов), веса человека.
Выделяют:
- Лёгкую степень: без потери сознания. Офтальмопатичекие признаки начинаются с пелены перед глазами, нечёткости зрения, расширения зрачков. Основные проявления желудочные (тошнота, боль в желудке); восстановление происходит через 3—5 суток.
- Средней тяжести (дополнительное название «офтальмическая»): все признаки более выражены. Но потери сознания нет. Ведущий симптом — нарушение зрения, слепота. Лёгкие нормально работают, гемодинамические показатели не ухудшаются.
- Тяжёлая с поражением всех органов и систем (генерализованная). После скрытой фазы быстро развёртываются неврологические симптомы, сильное возбуждение, рвота, боли в икроножных мышцах; влияние на сосудистую систему приводит к сердечной недостаточности (цианоз); нарушается дыхание; возникают судороги. Затем кома. Смерть возможна на фоне острого отёка мозга, острого панкреатита, декомпенсированного токсического шока. Летальный исход может наступить на 1—2 сутки.
Как проверить питьевой или нет в домашних условиях?
Существует несколько простых домашних способов отличить медицинский спирт от технического.
Поджигание жидкости
Некоторые наливают спирт в небольшую емкость, а некоторые просто смачивают ватную палочку в жидкости. Описываемая методика не требует специальных приспособлений, однако результат исследования — мгновенный и точный.
Этиловый спирт горит синим пламенем, а у метанола пламя всегда зеленого оттенка.
Стоит учитывать, что этот способ подходит только для различия чистых спиртов без примесей.

Проба картофелем
- Берут овощ небольшого размера, тщательно очищают и разрезают пополам.
- Затем корнеплод помещают в стеклянный сосуд и заливают спиртом.
- Оставляют картофель в таком виде на 3-4 часа.
- Если по истечению этого срока картофель не приобрел розовый цвет, то перед вами этиловый спирт — его можно применять в пищевой промышленности.
Использование соды
Добавьте немного соды в спирт. В том случае, когда в емкости находится этанол, сода станет желтого цвета и осядет на дне сосуда. В метиловом спирте сода растворяется полностью.
Марганцовкой
Подогреть спирт и добавить в него несколько гранул марганцовки. В пищевом спирте никаких изменений не произойдет. В нагретом метаноле марганцовка шипит и пенится.

Использование бытового градусника
Спирт нагревают в небольшой емкости (металлической). Во время кипения спирта измерьте его температуру. Температура кипения этанола — 80 градусов, а метилового спирта — 60 градусов.
Проведение пробы Ланга
Провести пробу Ланга (обесцветить жидкость):
- Взять небольшую емкость и налить туда спирт, который нагревают до 18 градусов.
- После этого в жидкость добавляют марганцовку и убирают с огня.
- После этого засекают временной период, через который жидкость из темно-малинового цвета перейдет в светло-розовый.
- Качество исследуемого спирта определяется по времени его осветления. Оптимальный период — 15-20 минут.
Формальдегидное исследование
Считается простым, но в то же время достоверным способом. Для проведения исследования спирт нагревают и помещают в него медную проволочку. Через 15 секунд медь достают и нюхают.

Чем больше выражен запах формальдегида, тем хуже качество спирта. Значит, употреблять такой спирт в пищу категорически нельзя.
ОПИСАНИЕ
Метанол — бесцветная легкоподвижная горючая жидкость, практически без запаха. Метанол смешивается во всех соотношениях с водой, этанолом, ацетоном, бензолом.
Молекулярный вес — 32,04.
Плотность — 0,8100 г/смВязкость — 0,817мПа-с
Температура кипения — 64,7 гр. С
Температура плавления — -97,68 гр.С
Теплота парообразования — 8,94 ккал/моль
Теплота сгорания: жидкого — 173,65 ккал/моль, газообразного — 177,40 ккал/моль.
Химические свойства
По химическим свойствам метиловый спирт — типичный одноатомный алифатический спирт: сочетает свойства очень слабого основания и еще более слабой кислоты.
С щелочными металлами реагирует с выделением водорода, образуя метилаты (например, CH3ONa); в реакции с кислотами образуются сложные эфиры (в присутствии сильных минеральных кислот реакция ускоряется), например с HNO2 дает метил-нитрит CH3ONO (количественно), с H2SO4 при температуре ниже 100 гр. С — метилсульфат CH3OSO2OH, с карбоновыми кислотами — RCOOCH3.
При взаимодействии с аммиаком в присутствии дегидратирующих катализаторов метанол дает метиламины.
Он разлагается водяным паром на катализаторе:
СН3ОН + Н2О = ЗН2 + СО2.
С воздухом образует взрывоопасные смеси (температура вспышки 15,6 гр.C).
Класс опасности — III. По степени воздействия на организм человека – умеренно опасное вещество
Смертельная доза метанола при приеме внутрь равна 30 г, но тяжелое отравление, сопровождающееся слепотой, может быть вызвано 5-10 г. Действие паров его выражается в раздражении слизистых оболочек глаз и более высокой подверженности заболеваниям верхних дыхательных путей, головных болях, звоне в ушах, дрожании, невритах, расстройствах зрения. Метанол может проникать в организм через неповрежденную кожу.
Предельно допустимая концентрация метанола в воздухе рабочей зоны равна 5мг/м.
Упаковка, транспортировка и хранение
Метанол транспортируют в специальных железнодорожных цистернах, автоцистернах, стальных бочках вместимостью 200 м3, пластмассовых емкостях или металлических бочках с наружным коробом из деревянных досок и стеклянных 20-ти литровых бутылях в соответствии с правилами перевозки грузов, действующими на данном виде транспорта.
При транспортировке необходимо соблюдать условия герметичности груза, защиты от падений и разрушений. Строго запрещается транспортировка метанола вместе с кислотами, кислотными ангидридами, сильными окислителями, щелочными металлами, легко воспламеняющимися и горючими веществами, химическими веществами для пищевой продукции.
Запрещаются остановки транспортного средства с грузом вблизи жилых районов и скоплений людей.
Продукт хранят в герметичных емкостях, в затененных проветриваемых складских помещениях вдали от источников тепла, искр, попадания прямых солнечных лучей, отдельно от окислителей. Температура хранения не должна превышать 30ºС.
Гарантийный срок хранения метанола – 6 месяцев.
Применение
Метанол — один из ключевых продуктов химической промышленности, который
является сырьем для получения многих продуктов органического синтеза.
Главные сферы применения метанола:
производство формальдегида (участвующего в синтезе
различных пластмасс) и МТБЭ (высокооктановой присадки к моторному топливу).
в производстве синтетических каучуков, уксусной кислоты, метилметакрилата, пластмасс, растворителей, метиламинов, диметилтерефталата, метилформиата, хлористого метила.
для получения лекарственных средств;
как добавка к автомобильным бензинам;
как денатурирующая добавка к этиловому спирту, предназначенного для промышленного использования;
в последнее время метанол находит применение в топливных элементах;
как промышленный растворитель;
метанол входит в состав ряда антифризов.
Виды спирта и характеристики
Этиловый
Этиловый спирт представляет собой бесцветную прозрачную жидкость. Он обладает характерным слабым запахом и ярко выраженным жгучим вкусом,
Чистый этиловый спирт, который применяют в химической отрасли, отличается нейтральными реакциями. А вот тот этанол, который используется в пищевой промышленности, смешивается с дополнительными элементами и поэтому обладает слабой реакцией.
Этил с нормальным давлением закипает при нагревании до 78,3 градусов. Стоит отметить, что с повышением температуры жидкости её плотность уменьшается.
При приеме небольшого количества жидкости человек ощущает легкое опьянение, а вот при приеме большого количества этанола состояние организма сходно с наркозом.

Запах спирта также опасен для живого организма. Показатели допустимой нормы не должны превышать 1000мг/м3. Опасная токсическая концентрация — свыше 1600 мг\м3. Запах спирта в помещении ощущается при концентрации в 250 мг/м3.
Этанол соединяют с водой в любых пропорциях:
- Во время этого процесса повышается температура жидкости, и полученное тепло выделяется в воздух.
- Спирт обладает летучестью, поэтому, ели хранить водно-спиртовой раствор в открытой светлой емкости, то со временем содержание спиртов в смеси уменьшается.
Этанол легко воспламеняется и горит светло-голубым пламенем. При распаде продукта выделяется углекислый газ и вода.
Получить этанол можно и в домашних условиях. Для этого используют специальный самогонный аппарат.
При длительном употреблении продуктов, содержащих спирт, возникает алкогольная зависимость
Поэтому употреблять спиртосодержащие напитки нужно с особой осторожностью
Что такое этанол и как получить его в домашних условиях рассказывается на видео:
Метиловый
Жидкость является представителем простейших одноатомных спиртов.
В различных источниках продукт именуют по-разному:
- гидроксидом метила,
- метанолом,
- древесным спиртом,
- карбинолом,
- метилгидратом.
Метанол — это бесцветная жидкость, которая по запаху схожа с этиловым спиртом. При смешивании с водой может расширяться или сжиматься.

Жидкость зарекомендовала себя в качестве хорошего растворителя, поэтому ею нередко заменяют этиловый спирт.
Аромат у метила очень слабо выражен, ощутить его возможно только при «принюхивании».
Во время работы с метанолом необходимо строго соблюдать все правила безопасности, поскольку неосторожная работа приводит к ожогам кожных покровов.
Сейчас метанол получают следующим способом:
- Синтезируют оксид углерода и водорода.
- Весь процесс происходит при температуре 250 градусов выше нуля.
- Давление должно быть в пределах 7 мегапаскалей.
- До этого момента метил получали путем сухой перегонки дерева.
- В редких случаях производители используют отходы нефтепереработки или коксующийся уголь.
При домашнем приготовлении спиртных напитков очень важно правильно подобрать вид спирта. Неправильный выбор продуктов приготовления приводит к сильным пищевым отравлениям

Риск приобрести некачественную водку возрастает в том случае, если вы приобретаете её в незарегистрированных торговых точках или на привокзальных площадях. А вот в больших официальных магазинах в 99% случаев продается лицензионный алкоголь.
Как отличить этиловый спирт от метилового в домашних условиях?
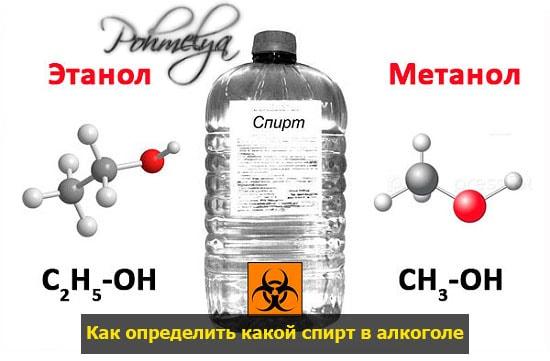
Итак, как определить метиловый спирт в домашних условиях, есть ли он в алкоголе или любом другом составе либо нет?
Опираться на один лишь вид или запах – нельзя. Оба спирта – это бесцветная жидкость, имеют похожий вкус и аромат (у метилового он, правда, не настолько насыщенный).
Если вы химик или увлекались этой наукой – вы сможете определить по запаху, есть ли в составе ядовитая жидкость или нет.
Существует несколько вариантов:
- Вам понадобится очищенный картофель. Исследуемая жидкость. Картофель необходимо погрузить полностью в жидкость. В случае, если в ней содержится метанол – картофелина станет розовой. Если картофель будет синего оттенка либо останется без изменений – у вас медицинский или пищевой спирт.
- Проверить можно при помощи огня. Подожгите жидкость и понаблюдайте, какого цвета пламя. Если синего цвета – перед вами пищевой, если зеленого – метиловый.
- Подогрейте исследуемую жидкость в емкости из металла. Замерьте температуру кипения. Технический метанол имеет температуру кипения – 64 градуса. Пищевой этанол закипает при 78 градусах.
- При помощи медной проволоки, которую необходимо поджечь и погрузить в исследуемую жидкость. Если в ней присутствует хоть небольшое содержание СН3ОН – сразу же появится сильный неприятный запах (его можно сравнить с запахом слегка испорченных яблок либо уксусным ароматом). Этанол не пахнет таким ароматом.
- В исследуемую жидкость бросьте небольшое количество обычной пищевой соды. Тщательно все перемешайте. Понаблюдайте, есть ли в жидкости осадок? Какой он? Если остался и не растворился осадок желтого цвета – это значит, что в сосуде содержится этанол, который дает этот осадок при реакции с йодом. Если пищевая сода растворилась полностью и жидкость стала прозрачной – перед вами сосуд с большим содержанием в своем составе метанола.
Качество метилового спирта (и не только технического) можно определить и при помощи «пробы Ланга». Для этого исследования возьмите 50 мл спирта, предварительно налитого в посуду, которую можно подогревать, а также 2 мл марганцовки (перманганата калия).
Вы можете предварительно подготовить раствор марганцовки – 0,2 г сухой смеси нужно развести в дистиллированной воде.
Нагрейте исследуемую жидкость до 18 градусов Цельсия, влейте раствор марганцовки и тщательно взболтайте. Дальше необходимо считать время, за какой промежуток окрас жидкости изменится с насыщенного почти черного до желтовато розового оттенка.
Тест Ланга покажет насколько качественный спирт. Чем лучше качество – тем длиннее будет процесс того, как меняется оттенок. Тест считается пройденным, если жидкость обесцветилась не менее чем за 10 минут исследований.
К сожалению, все способы обнаружения СН3ОН в жидкости работают только лишь, если его там более чем половина всего объема.
В случае, если вы хотите приобрести алкоголь и есть сомнения относительно состава – рекомендуем все-таки приобретать такие напитки исключительно в магазинах, которые вызывают доверие. Гораздо больше шансов обнаружить подделку в небольших сомнительных точках продажи.
Что такое летальный синтез?
Ему подвергается до 95% метанола. Это биотрансформация метилового спирта в формальдегид. Продукт, в 30 с лишним раз более токсичный. Формальдегид окисляется в муравьиную кислоту. Выводятся метаболиты и часть неизменённого метанола в основном почками (ещё лёгкими, потовыми железами). Концентрация метаболитов в крови выше, чем исходного яда. Основная переработка производится в печени ферментом алкогольдегидрогеназой (АДГ). Она метаболизирует и этанол, но превращение метилового спирта идёт в 7 раз медленнее, поэтому токсическое влияние на организм растягивается на несколько суток.

Можно ли отравиться этанолом?
Небольшой дозой этанола отравляются в редких случаях. Отравление происходит только в том случае, если человек употребляет большое количество спиртных напитков.
Этапы опьянения:
- После первой выпитой рюмки алкоголя человек становится чересчур расслабленным, общительным. При этом физически никаких изменений не произошло, спирт повлиял только на работу головного мозга. Это и есть первые признаки этилового отравления. Содержание алкоголя в крови колеблется в пределах 0,3 — 1,0 промилле.
- Если человек продолжает прием алкоголя, общительность сменяется на наглость, повышается самооценка, проявляется возбудимость в легкой степени. Человек плохо справляется с координацией движения и реальной оценкой ситуации. Уровень алкоголя — 1,0 — 1,4 промилле.
- Следующий этап опьянения — покачивание во время ходьбы, искажение реального восприятия ситуации, а также периодическое желание спать. Иногда возникает тошнота. Зачастую человек проявляет гнев, страх или апатию. Сам человек отрицает факт алкогольного опьянения. Уровень спирта в крови — 1,8 промилле.
- Когда алкоголь доходит до отметки 2,0 — 2,4 промилле, мозг человека не способен контролировать свои движения. Реакция замедленная, а в некоторых случаях и вовсе отсутствует. Опьяненный не различает цвета, формы, расстояние и высоту. Речь становится невнятной, боль практически не ощущается.
- Если человек продолжает принимать алкоголь, уровень спирта в крови достигает 2,5 — 3,2 промилле. Человек полностью теряет контроль над своим телом, он может уснуть в любом положении и месте. При этом дальнейший прием алкоголя сопровождается тошнотой. Позывы к мочеиспусканию не ощущаются, поэтому все процессы происходят бесконтрольно.
- При уровне алкоголя 3,2 -4,0 промилле все рефлексы человека подавлены, а иногда и полностью отсутствуют. Кровообращение и дыхание нарушается, что приводит к коме или смерти.
Если уровень алкоголя превышает 4,0 промилле, ЦНС перестает работать, из-за чего дыхательные пути перестают работать. Все эти негативные процессы приводят к гипоксии (удушью) и мгновенной смерти.

Похмелье — оказание первой помощи
Если пьяного человека тошнит, дайте ему очистить желудок. Если опьяненный в состоянии пить, напоите его как можно большим количеством воды. Внимательно следите за тем, что человек не захлебнулся водой или рвотными массами.
После того, как человек проспится, ему понадобятся:
- одна таблетка ацетилсалициловой кислоты и анальгина (можно заменить аспирином и цитрамоном) — это поможет снять головную боль;
- любой вид сорбента (активированный угол или энтеросгель);
- большое количество питья — можно давать обычную минеральную воду и сладкие напитки (они особо необходимы, потому что во время рвоты организм теряет глюкозу);
- при слабых позывах к рвоте вызовите их искусственно, но перед этим выпить 200-250 мл теплой воды;
- контрастный душ, проветривание комнаты и прогулки на свежем воздухе;
- для ускорения работы желудка напоите больного куриным бульоном, накормите легким супом, овсяной кашей, зеленью или сырым яйцом.
Как быстро снять похмельный синдром рассказывается на видео:
Если у вас возникают сомнения в качестве приобретаемой алкогольной продукции, лучше проверить его качество несколькими способами одновременно.
Помните, что большое количество алкогольной продукции вредит вашему здоровью.
Головы, хвосты и промежуточные примеси
Принято разделять дистиллят на три фракции — головы, тело и хвосты. Раз вы добрались до этой статьи, значит вам это уже хорошо известно, но я все-таки напомню.
- Головы идут вначале. В основном это эфиры и альдегиды, поэтому головы также называют эфирно-альдегидной фракцией (ЭАФ). Отличаются резким запахом. Довольно распространено мнение, что головы это примеси, имеющие температуру кипения ниже этилового спирта. На самом деле это не так.
- Тело это фракция, состоящая преимущественно из этилового спирта. Собственно то, что мы пьем.
- Хвосты. Идут в конце и имеют неприятный запах.
Если бы все было так просто, то мы бы выливали в раковину все, что идет из куба до температуры кипения этилового спирта, отбирали бы его и останавливали перегонку, когда температура перевалит за 78,15 градусов. Но тут есть два больших НО (второе НО самое большое):
- Все примеси начинают испаряться задолго до своей температуры кипения. Хвостовые фракции присутствуют и в головах и в теле, только в значительно меньших количествах. Например вода в больших количествах присутствует в дистилляте, хотя мы никогда не гоним самогон до 100 градусов в кубе.
- В многокомпонентной смеси температура кипения отдельной примеси отходит на второй план. Главную роль здесь играет коэффициент испарения конкретной примеси. Причем этот коэффициент не постоянен и зависит от концентрации этилового спирта в смеси. Другими словами один и тот же компонент (скажем метиловый спирт) при различных условиях может быть и головной и хвостовой фракцией.
Подведя итог можно сказать, что есть головные фракции, которые всегда идут раньше этанола, например уксусный альдегид. Есть хвостовые, такие как фурфурол. А есть примеси, поведение которых зависит от концентрации спирта в смеси. Эти фракции называются промежуточными.
Хочется отметить, что такое поведение очень неприятно для нас с вами. Получается мы отобрали головы, поменяли приемную емкость и приступили к отбору тела. Через какое-то время крепость спирта-сырца изменилась и какая-то гадость, которая по нашим представлениям в основной своей массе должна пойти в хвостах, вылезает вперед и начинает идти в приемную емкость.
Типичным представителем промежуточных примесей является изоамиловый спирт, являющийся основой сивухи.
Тема эта очень серьезная и заслуживает отдельной статьи. В ближайшее время я ее напишу.
Отравление этиленгликолем
Этиленгликоль содержится в: тормозной жидкости, антифризе, растворителях, средства для мытья стекол. При попадании этиленгликоля в организм в процессе его распада образуются гликолевая и щавелевая кислота, которые и определяют тяжелое течение отравления. Щавелевая кислота образует нерастворимые соли, которые закупоривают почечные канальцы, вызывая острую почечную недостаточность. Выраженные симптомы отравления возникают через 4-8 часов после употребления этиленгликоля. Симптомы: тошнота, повторная рвота, психическое и физическое возбуждение, тремор, судороги, угнетение сознания, кома. Через 2-3 дня после отравления возникают симптомы острой почечной недостаточности: острые боли в пояснице, животе, моча цвета «мясных помоев», уменьшение количества мочи.

Все мы знаем, из чего состоят спиртные напитки, что они содержат какой-то алкогольный спирт.
А знаете ли вы, что такое этил или метанол? И как отличить метиловый спирт от этилового?
Ответы на данные вопросы вы найдете ниже.
Итак, давайте найдем определение каждому из этих спиртов.
Этиловый спирт, его еще называют питьевым, медицинским или пищевым спиртом. Имеет химическую формулу С2Н5ОН (также известен под названием этанол), является основой практически всех качественных спиртных напитков.
Известны случаи в разных странах всего мира (в том числе и в Российской Федерации) отравления некачественными спиртными напитками. Не редки не только случаи, когда люди остаются инвалидами (к примеру, полностью лишаются зрения), но и смертельные исходы.
Во времена Советского Союза даже существовал плакат, где был изображен рабочий в черных очках и с палкой слепого. Надпись на плакате гласила – «Не пей технический спирт! Ослепнешь!»
Суррогаты или некачественные напитки с высоким содержанием алкоголя, создаются на основе метанола. Это спирт с высоким содержанием метанола. Имеет химическую формулу СН3ОН.
В отличие от этила, метиловый – это яд для человека
Именно поэтому очень важно знать, как отличить этиловый спирт от метилового без наличия под рукой специальных приборов в домашних обычных условиях
Свойства метилового спирта
Важнейшие свойства метилового спирта обусловлены наличием гидроксильных групп в его молекулах.
Физические свойства
| Свойство | Описание |
| Молярная масса | 32 г/моль |
| Плотность | 0,7918 г/см3 |
| Температура плавления | -97oС |
| Температура кипения | 64,7oС |
Метанол – это прозрачная, бесцветная, легковоспламеняющаяся жидкость с очень низкой температурой кипения. При очищении метиловый спирт теряет запах. Метанол хорошо растворяется в полярных растворителя, смешивается с водой в любых пропорциях. При растворении в воде между молекулами спирта и воды образовываются водородные связи. Наличие водородных связей между молекулами спиртов обуславливают относительно высокую в сравнении с углеводородами температуру кипения.
Химические свойства
Реакции с металлами. Метиловый спирт взаимодействует с щелочными металлами с выделением водорода и образованием солеобразных соединений:
В этой реакции спирт напоминает кислоту. Однако его молекула не диссоциирует с образованием катионов Водорода, а водный раствор метилового спирта не действует на индикаторы.
Дегидратация. Так называют реакцию отщепления воды от какого-либо соединения. При пропускании паров метилового спирта через раскалённую трубку получается C2H2 и другие продукты.
Заключение
Вот к таким выводам я пришел. Это только вводная статья, которая оставляет больше вопросов, чем ответов.
В дальнейшем я планирую более подробно изучить вопрос с коэффициентом испарения.
Процессы перегонки браги из различного сырья. Конечно приготовление зерновых и плодово-ягодных дистиллятов это своего рода искусство, которому научить невозможно. Но какие-то общие рекомендации выработать думаю можно. Точнее они наверняка уже есть — профильной литературы выпущено огромное множество и на форумах очень много полезной, хоть и разрозненной информации. Осталось ее только изучить, сгруппировать и выложить на блоге. Всего ничего
Надеюсь эта статья даст начало очень интересной серии — хочется изучить состав браг, сделанных из различного сырья и определить какие-то общие правила их перегонки.
P.S. Очень хотелось бы услышать комментарии людей, разбирающихся в химии. Может кто-то что-то добавит или поправит меня.
Всем пока!
Дорофеев Павел.





